CALDEIRA DE ALTA PRESSÃO – CONTROLE FOSFATO COORDENADO

CALDEIRA DE ALTA PRESSÃO – 3 FUNDAMENTOS DO TRATAMENTO DA ÁGUA
05/03/2021
LIMPEZA QUÍMICA
08/03/2021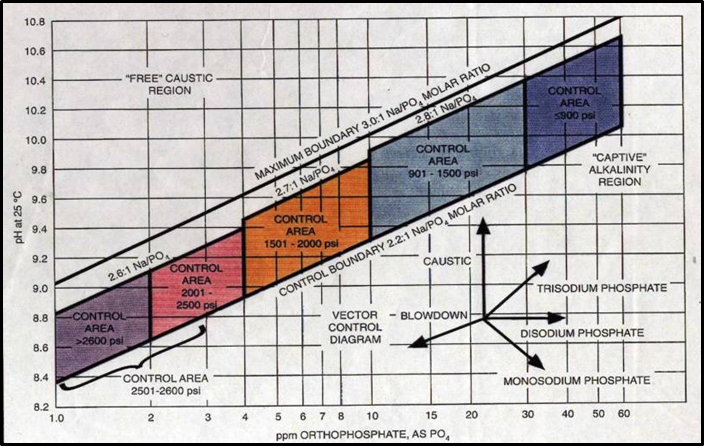
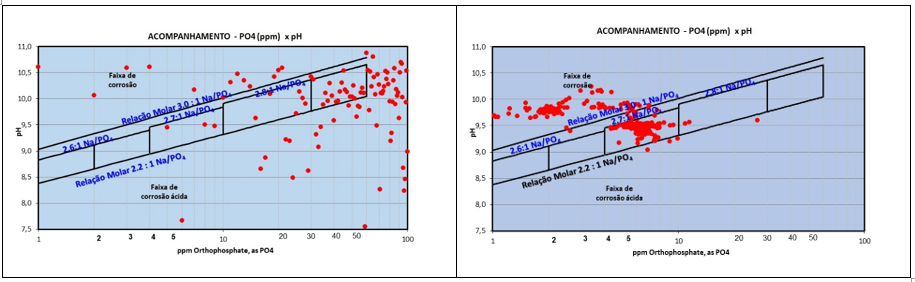
Se o controle da relação pH/PO4 da água de sua caldeira de alta pressão está como os apresentados nos gráficos 1 e 2, você tem sérios problemas no controle e monitoramento do tratamento químico e poderá ter surpresas muito desagradáveis no momento da inspeção ou pior, durante a operação do sistema.
O tratamento da água de caldeiras de alta pressão tem objetivo principal, evitar o processo corrosivo no equipamento, considerando a utilização de água de alimentação com qualidade físico-química adequada (ver nosso artigo relacionado: “CALDEIRA DE ALTA PRESSÃO – 3 FUNDAMENTOS DO TRATAMENTO DE ÁGUA“) e essa corrosão provocará certamente, sérios prejuízos e danos irreversíveis ao sistema como um todo e suas principais da corrosão nesses sistemas são: – oxigênio dissolvido – alta temperatura – ácido ou caustico
A água é a causadora da corrosão e a elevada temperatura acelera o processo corrosivo. Na ausência do oxigênio dissolvido (veja nossos artigos relacionados: DESAERAÇÃO e DESAERAÇÃO – Parte 2), teremos a seguinte a reação:
3Fe + 4H2O + CALOR –> Fe3O4 + 4H2
O produto desse tipo de corrosão é a magnetita (Fe3O4), que propicia a formação de uma película na superfície metálica que impede o contato direto entre a água e o metal, minimizando sensivelmente a corrosão, o que torna possível a utilização de aço carbono na fabricação de caldeiras. Desta forma, consideramos que a magnetita é vital para a operação e preservação da caldeira. A ilustração abaixo exemplifica esse processo:
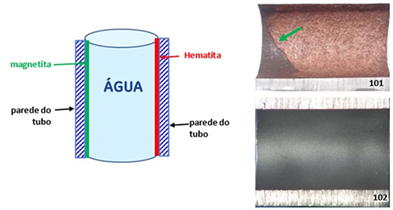
Haverá ainda, uma corrosão mínima que reconstrói a camada de magnetita danificada continuamente pelas alterações de temperaturas e ambiente dinâmico da caldeira.
A magnetita é produzida por uma sucessão de reações (ver nosso artigo relacionado: “CONTROLE DA CORROSÃO EM CALDEIRAS DE ALTA PRESSÃO“) e sua estabilidade depende principalmente do pH da água, pois tanto a presença de ácidos ou cáusticos provocam a corrosão e portanto, é imprescindível adotarmos uma faixa segura de pH para preservação da magnetita.
Devemos evitar ao máximo a operação da caldeira com pH ácidos pois nesta condição, a corrosão é muito rápida, principalmente nas regiões de temperaturas mais elevadas como na parede de água na fornalha. Em sistemas de pré-tratamento que utilizam troca ionica, devemos instalar instrumentação adequada de monitoramento capaz de detectar e desviar o fluxo de água antes que chegue ao desaerador, evitando assim, a contaminação da água da caldeira.
A corrosão por ácido, geralmente proveniente do sistema de regeneração das resinas, é muito conhecida e facilmente detectada através do monitoramento adequado do pH, mas a corrosão cáustica não é tão direta assim e não é necessário uma grande quantidade para provocar uma severo processo corrosivo, o que pode ocorrer mesmo em pH <12,7, considerado seguro, pois a concentração da água em uma área localizada como tubos próximos da zona de calor, pode provocar níveis elevados de cáusticos e a dissolução da camada protetora de magnetita, pois esses depósitos de ferro são porosos e permitem a passagem da água contendo esses cáusticos para a interface com o metal e a água ao evaporar, concentra esses cáusticos, podendo chegar a 10.000 ppm ou mais, dissolvendo a camada de magnetita deixando o aço exposto que reagirá com a água para nova formação da magnetita, mas enquanto houver o processo cáustico, o processo de dissolução da magnetita continua, provocando desgaste acelerado do tubo.
Os depósitos cáusticos geralmente são caracterizados por “estrias” sob os depósitos com coloração esbranquiçada, que geralmente é o carbonato de sódio.
O ataque cáustico é mais comum em sistemas que operam com pressões de 70 Kgf/cm² ou mais, mas existem casos comprovados que operavam com 28 Kgf/cm². As caldeiras de alta pressão são mais suscetíveis a esse tipo de corrosão em função dos seguintes fatores: – necessidade de água desmineralizada – o Hidróxido de Sódio utilizado na regeneração é o principal contaminante – Elevadas taxas de fluxo de calor – Maior temperatura de saturação
Outra forma de corrosão induzida por cáustico é a “fragilização”. A solução concentrada de cáustico ataca o aço provocando “fendas” por toda sua estrutura granular, que fragiliza drasticamente o metal e não é detectado previamente. O programa de tratamento com controle PO4/pH coordenado é o único método seguro para prevenirmos esse tipo de corrosão, pois atua evitando a concentração de cáustico no interior da caldeira e com isso, a tendência à fragilização. Essa neutralização do cáustico pelo PO4 ocorre pelas seguintes reações:
Na2PO4 + NaOH –> Na3PO4 + H2O ou HPO4= + OH– –> PO4= + H2O
A reação tenderá à direita com a elevação do pH e assim, se o PO4 suficiente estiver presente na água da caldeira para reagir com o OH–, a reação se torna “autolimitada”, ou seja, o pH não pode se elevar, pois toda OH– foi consumida pelo HPO4=.
O gráfico de relação de PO4/pH é utilizado para controle do programa de tratamento químico da água, que considera o pH x PO4 x pressão. O limite máximo representa o pH e as condições de concentração de PO4 onde existe residual de HPO4= suficiente para reagir com o OH– presente no meio. Acima desse limite, o pH ou a concentração de OH– é muito alta para a quantidade de HPO4= presente indicando assim, a presença de cáustico “livre”. Por outro lado, abaixo desse limite máximo, existe PO4= mais que suficiente para a reação com a OH– presente, indicando que o cáustico poderá ser “adsorvido”. O residual máximo de PO4 a ser mantido é limitado pela contribuição do PO4 na condutividade na água da caldeira e quanto maior a pressão, menor deverá ser o teor de PO4.
compartilhe esse artigo,
Se você deseja adquirir nossas apostilas de tratamento de águas de caldeiras e de resfriamento, acesse: www.brunharawater.com.br/contato
Este é um conceito básico que espero esclarecer esse tema, mas participe de nosso fórum e traga suas perguntas e dúvidas.
Obrigado por acessar nosso site.
Brunhara



